实验室固定成员彭涛教授团队在中科院一区期刊发表SCI论文
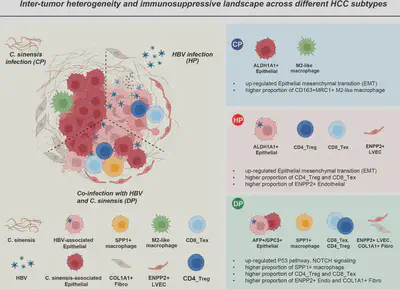
2026年1月5日,实验室固定成员、广西医科大学第一附属医院肝胆外科彭涛教授团队联合中国中医科学院王继刚教授、复旦大学卢国栋教授,中日友好医院贾立群教授以及广西医科大学周静教授团队在中科院一区期刊《Molecular Cancer》杂志发表题为“Integrating single cell- and spatial- resolved transcriptomics unravels the inter-tumor heterogeneity and immunosuppressive landscape in HBV- and Clonorchis sinensis-associated hepatocellular carcinoma” (整合单细胞和空间转录组学解析乙肝及华支睾吸虫相关肝细胞癌的肿瘤异质性与免疫抑制微环境)的研究论文。彭涛教授、王继刚教授、卢国栋教授、贾立群教授、周静教授为该论文共同通讯作者。
1、研究背景与目的
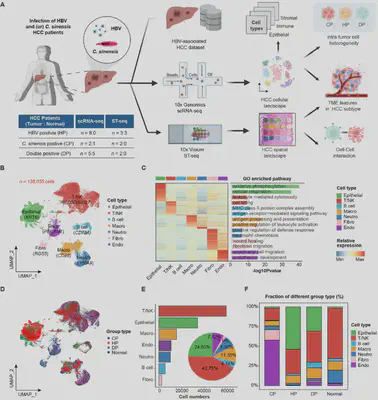
该研究聚焦乙型肝炎病毒(HBV)和华支睾吸虫(C. sinensis)感染相关的肝细胞癌(HCC),整合单细胞RNA测序(scRNA-seq)和空间转录组学(ST-seq)技术,系统解析不同感染背景下HCC的肿瘤间异质性及免疫抑制微环境特征。研究纳入269例原发性HCC患者队列,并结合21个样本的scRNA-seq数据(138,055个细胞)和10个样本的ST-seq数据(32,072个spots),旨在阐明单一感染(CP组:仅C. sinensis感染;HP组:仅HBV感染)与双重感染(DP组:HBV+C. sinensis共感染)在细胞组成、分子通路和空间架构上的差异。
2、核心研究内容
关键临床发现:C. sinensis感染显著恶化预后
临床分析显示,C. sinensis感染是HCC患者总生存期(OS)缩短的独立危险因素(HR=2.782, P=0.0159)。DP组中位OS仅68.32个月,显著短于CP组(75.11个月)和HP组(84.54个月),表明双重感染患者预后最差。这一结果凸显了C. sinensis感染在HBV相关HCC进展中的协同致癌作用。
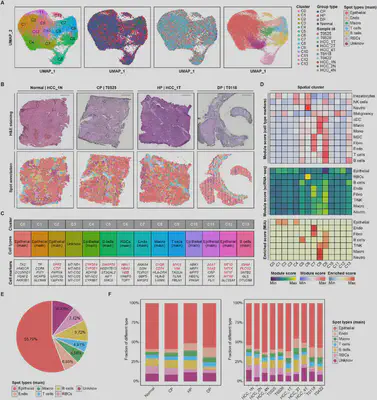
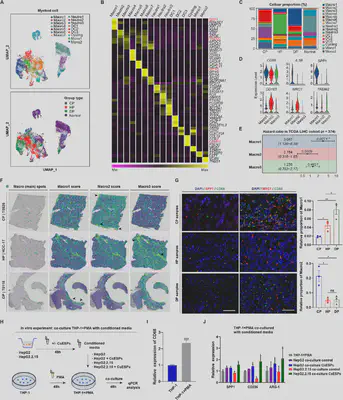
肿瘤细胞异质性:DP组呈现高度恶性特征
scRNA-seq分析鉴定出7种主要细胞类型,其中DP组肿瘤细胞表现出独特的分子图谱:在恶性标志物方面,AFP、GPC3和ARG-1水平显著升高,提示更强的侵袭性;基因组层面,染色体9+、10+、22+区域拷贝数变异(CNV)评分最高,显示出更严重的基因组不稳定性;通路激活谱上,DP组特异性激活p53、NOTCH、缺氧及PI3K-AKT-mTOR通路,而CP和HP组主要富集上皮-间质转化(EMT)通路;此外,DP组还高表达癌症干细胞相关基因(CD24、ANPEP),与免疫逃逸和耐药相关。空间定位验证通过免疫荧光(IF)染色证实,DP组p53/p21蛋白表达显著上调,从蛋白水平印证了转录组学发现。
免疫微环境异质性:SPP1+巨噬细胞主导DP组免疫抑制
髓系细胞重聚类鉴定出16个亚群,其中SPP1+肿瘤相关巨噬细胞(Macro1)在DP组显著富集,且具有独特的促炎表型,高表达IL1B和SPP1,与M2型(Macro2,高表达CD163/MRC1)和TREM2+巨噬细胞(Macro3)形成鲜明对比。临床相关性分析显示,TCGA队列中SPP1+巨噬细胞评分高的患者死亡风险增加3.087倍(P=0.0271)。空间共定位分析通过ST-seq和IF证实,DP组织中CD68+SPP1+巨噬细胞与肿瘤细胞紧密相邻,形成物理性免疫屏障。体外机制研究进一步揭示,HBV+C. sinensis分泌蛋白(CsESPs)联合刺激可诱导巨噬细胞向SPP1+极化,提示感染微环境直接驱动这一表型转换,从而构建具有更强免疫抑制功能的微环境。
T细胞耗竭状态:DP组CD8+ T细胞功能严重受损
淋巴细胞分析揭示DP组和HP组均富集耗竭型T细胞亚群,但DP组表现尤为突出。CD8+耗竭T细胞(CD8_Tex)在DP组耗竭评分最高,高表达LAG3、PDCD1(PD-1)、HAVCR2(TIM-3)等抑制性受体;CD4+调节性T细胞(CD4_Treg)在DP组比例增加,且表达更高水平的TIGIT和GNLY,协同抑制抗肿瘤免疫。伪时间轨迹分析显示,DP来源的CD8_Tex细胞主要分布于免疫抑制相关分支(cell fate 2),而HP组细胞多位于抗原呈递调控分支(cell fate 1),揭示双重感染特异性削弱T细胞功能,使其无法有效执行抗肿瘤免疫应答。空间分布分析显示,DP样本中LAG3/PDCD1/FOXP3表达强度在T细胞浸润区显著升高,从空间维度证实了免疫抑制微环境的形成。
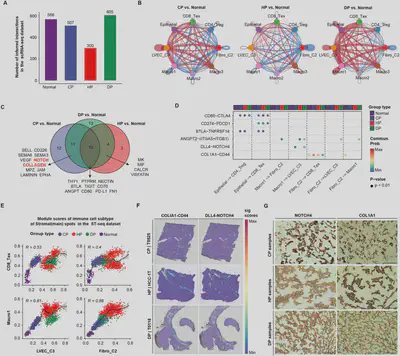
基质细胞与细胞互作网络重塑微环境
基质细胞(内皮细胞和成纤维细胞)呈现感染类型特异性分布:肝血管内皮细胞(LVEC_C3)在DP和HP组特异性富集ENPP2+亚型,与肝纤维化和血管生成相关;癌相关成纤维细胞(Fibro_C2,COL1A1+)在DP组富集,通过COL1A1-CD44配受体轴与CD8_Tex和SPP1+巨噬细胞形成强相互作用;NOTCH信号轴在DP组中表现为DLL4-NOTCH4配受体对在肿瘤细胞与LVEC_C3内皮细胞间显著上调,促进血管生成和干细胞维持。CellChat分析显示DP组细胞互作总数最高(605对),远超HP组(300对),提示双重感染构建更复杂的免疫抑制网络,其中COL1A1-CD44和DLL4-NOTCH4是关键的功能性。
研究首次绘制了HBV和C. sinensis单一/双重感染HCC的多维细胞图谱,揭示DP组通过"SPP1+巨噬细胞-耗竭T细胞-促纤维化成纤维细胞"三重机制构建强效免疫抑制微环境,其肿瘤细胞表现出更高的恶性程度和基因组不稳定性。基于这些发现,研究提出分型治疗策略:DP患者可优先采用p53功能恢复疗法联合SPP1+巨噬细胞重编程;CP/HP患者适合靶向EMT通路。在免疫治疗方面,DP组PD-1抑制剂与TIM-3/LAG-3阻断剂联用可能增强疗效。此外,SPP1+巨噬细胞比例、ENPP2表达水平和CD8_Tex耗竭评分可作为DP患者风险分层的生物标志物。尽管研究存在ST-seq分辨率限制、未纳入治疗反应数据等局限,这些发现仍为感染相关HCC的精准诊疗提供了重要的理论依据和潜在靶点,深化了对不同感染类型HCC异质性多细胞生态系统的理解。